
 |
Glaucoma |
Grupo de enfermedades caracterizadas por una lesión progresiva del nervio óptico debida, al menos parcialmente, al aumento de la presión intraocular.
La presión intraocular (PIO) normal varía entre 11 y 21 mm Hg; no obstante, estos niveles pueden llegar a ser excesivos en algunas personas, que pueden desarrollar lesión del nervio óptico con una presión intraocular normal (glaucoma de tensión normal o baja). Por otro lado, hay muchos pacientes con presiones >21 mm Hg sin lesiones en el nervio óptico (hipertensión ocular).
 |
|
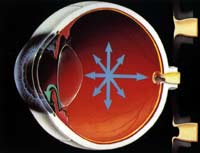
Aumento
de la presión intraocular
|
Incidencia
El glaucoma es la segunda causa de ceguera en Estados Unidos. Alrededor de 2 millones de estadounidenses padecen glaucoma, aunque aproximadamente la mitad lo ignoran. A pesar de que el glaucoma se considera una enfermedad del envejecimiento, puede ocurrir en cualquier grupo de edad. De los pacientes con hipertensión ocular, solamente un1% anual desarrollará glaucoma.
Patogenia
El glaucoma puede clasificarse según la existencia de obstrucción en el sistema de drenaje como glaucoma de ángulo abierto o de ángulo cerrado (glaucoma por cierre angular). Además, puede subdividirse según su etiología en primario o secundario (v. tabla 100-1).
El principal sistema de drenaje (convencional) del ojo se localiza en el ángulo de la cámara anterior y se encarga del 83-96% de este drenaje en condiciones normales. Consiste en el flujo de humor acuoso a través de la malla trabecular, el canal de Schlemm, los canales intrasclerales y las venas episclerales y conjuntivales. En el glaucoma de ángulo abierto con aumento de la PIO, la elevación de la tensión se debe a que el drenaje es inadecuado a pesar de que el ángulo se mantiene abierto y parece relativamente normal en la exploración gonioscópica. En el glaucoma de ángulo cerrado, el aumento de la PIO se produce cuando el drenaje normal del acuoso fuera del ojo disminuye en grado suficiente por una obstrucción física del iris periférico. Las vías secundarias (alternativas) de drenaje del humor acuoso, también conocidas como sistema de drenaje uveoscleral, eliminan el 5-15% del humor acuoso formado. Consiste en la salida de humor acuoso a través de la cara anterior del cuerpo ciliar y los músculos ciliares hasta alcanzar el espacio supracoroideo (p. ej., entre la coroides y la esclera), donde abandona finalmente el ojo a través de canales esclerales.
Diagnóstico
Es esencial una exploración oftalmológica exhaustiva para realizar precozmente el diagnóstico y el tratamiento. Debe incluir la visualización del ángulo mediante un prisma o lente de contacto especial (gonioscopia), la medida de la PIO, la exploración del campo visual y, sobre todo, el examen del nervio óptico. Una prueba de detección selectiva de glaucoma basada sólo en la toma de la PIO tiene poca sensibilidad, especificidad y valor predictivo positivo. Los pacientes con riesgo de glaucoma deben remitirse al oftalmólogo para una exploración completa.
La visualización del ángulo de la cámara anterior permite diferenciar entre el glaucoma de ángulo abierto y de ángulo cerrado. No obstante, al ser opacos el limbo y la esclera situados por encima, el ángulo sólo puede verse mediante gonioscopia.
Si la decisión de tratar el glaucoma se basa sólo en el aumento de la PIO, algunos pacientes con glaucoma de tensión normal se verán privados del tratamiento que precisan, mientras que otros con hipertensión ocular recibirán un tratamiento innecesario de por vida que les puede causar efectos secundarios. Alrededor del 90% de los pacientes con hipertensión ocular (>21 mm Hg) nunca desarrollarán glaucoma. Aunque muchas personas con hipertensión ocular pueden tolerar niveles tensionales elevados, si la PIO excede de 27-30 mm Hg conviene iniciar el tratamiento, sobe todo en personas con factores de riesgo asociados.
GLAUCOMA PRIMARIO DE ÁNGULO ABIERTO
Glaucoma asociado a un ángulo de la cámara anterior abierto.
El glaucoma primario de ángulo abierto es la forma más corriente de glaucoma, responsable del 60-70% de todos los casos. Suelen afectarse ambos ojos, aunque puede ser de modo asimétrico. Los factores de riesgo para el glaucoma primario de ángulo abierto se enumeran en la tabla100-2.
Glaucoma de presión normal o baja: Al menos la sexta parte de los pacientes con glaucomas tienen una PIO dentro de los límites normales. Estos pacientes muestran una pérdida campimétrica típica de glaucoma. El tratamiento se basa en disminuir la PIO, aunque ésta sea «normal», ya que resulta demasiado elevada para ese ojo y contribuye al daño del nervio óptico. Existen causas variadas para los glaucomas de tensión baja o normal, al igual que sucede con los glaucomas con aumento de la PIO. En algunos pacientes, la lesión del nervio óptico puede ser producida más por un aporte sanguíneo inadecuado que por la PIO. Los defectos campimétricos con frecuencia son más profundos y localizados, originando escotomas paracentrales. Estos pacientes tienen mayor incidencia de migraña que la población general, lo que sugiere una posible etiología vasospástica.
Síntomas y signos
Generalmente no hay síntomas precoces. Cuando el paciente se da cuenta de la pérdida de campo visual, el grado de atrofia del nervio óptico suele ser muy acusado. La visión central es habitualmente la última en afectarse, perdiéndose primero la visión periférica de forma asintomática. No obstante, algunos pacientes pueden referir síntomas, como problemas al bajar escaleras si se afecta el campo visual inferior, dificultad para conducir o pérdida de algunas palabras cuando leen.
Diagnóstico
Los hallazgos diagnósticos en la exploración incluyen un ángulo abierto y normal en la gonioscopia, el aspecto de la papila óptica y un campo visual característico de glaucoma, así como asimetría de la PIO en la mayoría de los casos, siendo ésta mayor en el ojo con lesión más avanzada del nervio óptico. La PIO puede ser normal o elevada.
Antes de establecer un diagnóstico de glaucoma de presión normal, deben descartarse los siguientes factores: toma inadecuada de la PIO, grandes fluctuaciones diurnas, antecedentes de PIO elevada (glaucoma «quemado»), cierre angular intermitente, corticoterapia previa con aumento de la PIO, antecedentes de crisis hemodinámicas o enfermedades cardiovasculares y cualquier otro trastorno ocular o neurológico que pueda producir defectos campimétricos similares en la capa de fibras nerviosas.
La frecuencia de las revisiones en pacientes con hipertensión ocular (PIO elevada con campos y papilas normales) depende en parte de los factores de riesgo adicionales, como edad, raza, historia familiar, miopía y diabetes.
La frecuencia de los exámenes de revisión varía de semanas a años, dependiendo de si el paciente tiene glaucoma o riesgo de glaucoma, si es fiable o de la gravedad del glaucoma, así como del grado de respuesta al tratamiento. En ocasiones, hay que medir la PIO cada semana o cada mes, mientras que otras veces basta hacerlo cada 1 o 2 años. El examen del campo visual debe repetirse cada 1-6 meses, o solamente cada 1-3 años en pacientes estabilizados. Se obtendrán fotografías seriadas del nervio óptico para determinar si avanzan las lesiones. Si hay progresión, el nivel terapéutico de PIO seleccionado para ese paciente debe ser rebajado e iniciarse un tratamiento adicional.
Tratamiento
El objetivo del tratamiento médico, con láser o quirúrgico, es prevenir las alteraciones glaucomatosas del nervio óptico y del campo visual estabilizando la PIO. La pérdida visual por glaucoma no se puede corregir. El tratamiento intenta bajar la PIO hasta un nivel terapéutico, alrededor de un 30-40% inferior al nivel que se cree que provoca daños en el nervio óptico. Es muy útil obtener una línea base mediante diferentes pruebas como campimetría, fotografía del nervio óptico y dibujos detallados del mismo, para realizar comparaciones futuras.
Con frecuencia, el tratamiento inicial del glaucoma es farmacológico (v. tabla 100-3) o mediante láser. Si estos tratamientos fracasan o se prevé que lo hagan, se puede considerar la cirugía de filtración. No obstante, hay ciertas situaciones (especialmente si la medicación no puede tolerarse) en las que se empieza con cirugía de filtración.
Con el advenimiento de nuevos fármacos, como los agonistas A2 adrenérgicos tópicos, los inhibidores de la anhidrasa carbónica tópicos o los análogos de prostaglandinas tópicos, se está produciendo un cambio gradual en el tratamiento médico.
Los pacientes que se administran antiglaucomatosos tópicos deben aprender a realizar el cierre pasivo de los párpados con oclusión del punto lagrimal para reducir la absorción sistémica y los efectos secundarios asociados. Los efectos colaterales de los betabloqueantes tópicos (timolol, levobunolol, carteolol, metipranolol, betaxolol) comprenden broncospasmo y falta de aliento -que los pacientes atribuyen con frecuencia a sobreesfuerzos-, depresión y fatiga -que muchos pacientes achacan a su edad-, confusión, impotencia, caída de cabello, hipoacusia y bradicardia. El médico debe preguntar sobre estos efectos secundarios porque pueden ser insidiosos y no asociarse con la medicación. El paciente a veces debe suspender durante períodos breves su tratamiento para averiguar si ésta es la causa de dichos síntomas.
Los agonistas adrenérgicos no selectivos tópicos (adrenalina y dipivefrina) presentan una alta incidencia de reacciones tóxicas o alérgicas y en muchos pacientes no consiguen reducir la PIO. No obstante, pueden ser beneficiosos en ciertos pacientes. Los agonistas adrenérgicos A2 selectivos (apraclonidina y brimonidina) bajan eficazmente la PIO, aunque, debido a la alta frecuencia de reacciones alérgicas y de taquifilaxia, la apraclonidina parece más útil en la prevención de las elevaciones de PIO postláser y posquirúrgicas y al control tensional a corto plazo más que para tratamientos prolongados. Las reacciones alérgicas y la taquifilaxia parecen menos frecuentes con la brimonidina, aunque algunos pacientes pueden sufrir sequedad de boca. Los agonistas colinérgicos tópicos (p. ej., pilocarpina, fosfolina) siguen siendo una opción excelente en ciertos pacientes, como los seudofáquicos en los que ni la miosis ni la catarata son ya un problema. Los inhibidores de la anhidrasa carbónica orales (p. ej., acetazolamida, metazolamida) son muy eficaces en la reducción de la PIO, pero sus frecuentes efectos secundarios -como fatiga, anorexia, depresión, parestesias, alteraciones electrolíticas en plasma, litiasis renal o discrasias sanguíneas- limitan su empleo. La dorzolamida, un nuevo inhibidor tópico de la anhidrasa carbónica, baja la PIO sin inducir los efectos colaterales asociados con los inhibidores orales. Algunos pacientes que reciben inhibidores tópicos de la anhidrasa carbónica se quejan de sabor amargo tras la instilación de las gotas. El latanoprost, análogo tópico de prostaglandinas, reduce eficazmente la PIO durante 24 h con una única aplicación diaria. Parece ser bien tolerado y presentapocos efectos sistémicos; el principal efecto secundario ocular es el aumento de la pigmentación del iris, especialmente en los iris de colorverdoso, y un posible empeoramiento de las uveítis.
El tratamiento quirúrgico del glaucoma primario de ángulo abierto y del glaucoma de tensión normal incluye la trabeculoplastia con láser o un procedimiento de filtración protegido y posiblemente el empleo de tubos de drenaje o procedimientos ciclodestructivos.
La trabeculoplastia con láser de argón puede realizarse como tratamiento inicial, en pacientes en los que el tratamiento médico fracasa o que no toleran la medicación. Se aplican impactos de láser en 180 o 360º de la malla trabecular para mejorar su función y reducir de este modo la PIO. Al cabo de 2 a 5 años, el 50% de los pacientes requerirán tratamiento médico o quirúrgico adicional debido al insuficiente control de la PIO.
El procedimiento quirúrgico más empleado es una intervención de filtración protegida. Se realiza un agujero de espesor parcial en la esclera que permite el drenaje del humor acuoso de forma controlada para almacenarse bajo la conjuntiva, formando una ampolla de filtración. Estos pacientes presentan un riesgo mayor de endoftalmitis y se les debe instruir para que comuniquen inmediatamente cualquier síntoma o signo de infección de la ampolla o de endoftalmitis.
GLAUCOMA POR CIERRE ANGULAR
Glaucoma asociado a ángulo de la cámara anterior cerrado.
El glaucoma por cierre angular representa el 10% de todos los glaucomas en Estados Unidos. Puede ser primario, por bloqueo pupilar, o secundario, debido a tracción del iris hacia el ángulo o a lesiones que empujan el iris hacia delante. Las dos situaciones más frecuentes en las que el iris es arrastrado hacia el ángulo son el glaucoma neovascular en pacientes con diabetes u oclusión de la vena central de la retina, y los precipitados inflamatorios que provocan sinequias anteriores del iris en el ángulo. Hay muchas etiologías posibles que pueden empujar el iris hacia delante y producir cierre angular, siendo la más frecuente el bloqueo pupilar primario, sobre el que se centrará el resto de este apartado.
La prevalencia de glaucoma primario por cierre angular difiere según el grupo étnico o racial. Es muy frecuente entre los esquimales y los asiáticos. El cierre angular primario es más común en las mujeres, los hipermétropes y los ancianos, así como en pacientes con historia familiar de glaucoma de ángulo cerrado.
Durante el envejecimiento normal, el cristalino se vuelve más grueso, produciendo una mayor aposición con el borde pupilar. En los ojos anatómicamente predispuestos, este fenómeno puede impedir el flujo del humor acuoso desde la cámara posterior hacia la anterior, lo que origina un aumento de presión en la cámara posterior. Esta diferencia de presión provoca que el iris periférico se abombe hacia delante, obstruyendo el ángulo y causando cierre angular. El ángulo se puede ocluir parcial o intermitentemente, lo que puede provocar glaucoma por cierre angular intermitente, subagudo o crónico. Además, el ángulo puede quedar bloqueado completamente de forma brusca, lo que desencadena un glaucoma agudo. La raza y ciertas características anatómicas del ojo determinarán quién desarrollará glaucoma por cierre angular agudo o crónico.
Síntomas, signos y diagnóstico
La mayoría de las personas predispuestas al glaucoma por cierre angular agudo, crónico, subagudo o intermitente no tienen signos ni síntomas. No obstante, algunos pueden presentar signos sutiles, como enrojecimiento ocular, dolor, visión borrosa o cefalea. En ocasiones, estas molestias oculares mejoran al dormir, quizá debido a la miosis inducida por el sueño, que puede resolver un ataque intermitente o subagudo de glaucoma.
Los síntomas de glaucoma agudo por cierre angular son por lo general evidentes: dolor ocular intenso, hiperemia, descenso de visión, visión de halos coloreados, cefalea, náuseas y vómitos. Los pacientes que acuden a urgencias con un ataque de glaucoma agudo a veces son diagnosticados erróneamente, atribuyéndose sus síntomas a problemas neurológicos o gastrointestinales. La exploración de un paciente con glaucoma agudo revela la presencia de lagrimeo, edema palpebral, inyección conjuntival, velamiento corneal, pupila fija en semimidriasis y con frecuencia una inflamación leve en cámara anterior. Puede ser complicado realizar la gonioscopia a causa de la opacificación corneal; no obstante, la exploración del otro ojo mostrará un ángulo estrecho susceptible de ocluirse. Si el ojo contralateral presenta un ángulo completamente abierto, deben considerarse otros diagnósticos en vez de glaucoma por cierre angular.
Tratamiento
El tratamiento de un ataque agudo de glaucoma se debe iniciar inmediatamente, porque puede instaurarse con rapidez una pérdida de visión definitiva. El tratamiento inicial es médico: betabloqueantes tópicos, inhibidores de la anhidrasa carbónica tópicos, orales o i.v., y agonistas A2 adrenérgicos selectivos. Debe usarse un agente osmótico (v. tabla 100-3) si no se produce una respuesta adecuada. A continuación se añade pilocarpina al 1-2% dos veces, con 15 min de intervalo. Los mióticos no suelen ser efectivos si la PIO es >40-50 mm Hg, debido a anoxia del esfínter pupilar.
La iridotomía periférica con láser es el tratamiento definitivo del glaucoma agudo. Si la córnea no es transparente o el ojo se encuentra excesivamente inflamado, la iridotomía debe demorarse; en caso contrario se realiza lo antes posible. Como el otro ojo tiene un riesgo del 80% de desarrollar un ataque de glaucoma agudo, debe realizarse una iridotomía profiláctica en ese ojo.
El tratamiento definitivo en pacientes con glaucoma por cierre angular intermitente, subagudo o crónico también es la iridotomía periférica con láser. Además, debe realizarse una iridotomía periférica en pacientes en los que se detecte un ángulo potencialmente ocluible mediante gonioscopia, incluso en ausencia de síntomas, para prevenir el glaucoma por cierre angular.
El riesgo de complicaciones de la iridotomía periférica con láser es extremadamente bajo en comparación con sus efectos beneficiosos. Es posible que se presente diplopía, que puede ser molesta, si la iridotomía no se hace suficientemente periférica como para que la cubra el párpado superior. Puede producirse una hemorragia, aunque generalmente es autolimitada y sin consecuencias.
Tratamientos:
![]() Imagenes
Imagenes
Canales: Biblioteca Virtual | Apuntes | Provas de Residencia | Periodico médico | Links | E-Mail | Inicio
editora: Simone A. Beloto